[헬스컨슈머] 최근 셀트리온에서 개발한 코비드19 치료제 ‘CT-P59’가 ‘치료 목적 사용승인’을 받으면서, GC녹십자의 치료제 ‘GC5131’의 뒤를 이어 두 번째 국내 치료제가 되었다. ‘치료 목적 사용승인’ 이란 무엇인지, 그리고 녹십자에서 개발한 ‘GC5131’ 랑은 어떤 차이가 있는지 알아보자.

[치료 목적 사용승인]
치료목적 사용승인이란 생명이 위급하지만 대체 치료 수단이 없는 환자에게 임상시험 중인 의약품을 사용할 수 있도록 승인하는 제도를 말한다.
원래 의약품은 전임상시험 및 임상시험을 1상, 2상, 3상을 거친 후, 식품의약품안전처의 허가를 받은 다음 실제 환자들이 사용할 수 있다. 이 기간은 10년 이상 걸리기도 하기 때문에, 위급한 환자들이 현재 임상시험 중인 약을 투약하는 것이 치료적 유익성이 더 크다고 판단이 될 때, 사용할 수 있도록 만든 제도이다. 임상시험용 약품의 동정적 사용제도는 <약사법>의 제 34조 제 4항에서 허용되고 있다.

[셀트리온 ‘CT-P59’ 와 녹십자 ‘GC5131’가 가지는 의의]
이 두 약물 이전에 코로나19 치료목적으로 임상시험 승인을 받은 약물들은 이미 다른 적응증으로 허가를 받아 다른 질병에 사용하고 있는 약물을, 코로나19 에도 치료 효과가 있는지 시험을 하는, ‘약물재창출’ 방식으로 임상시험 승인을 받았다. 이 두 약물은 기존 약들처럼 ‘약물재창출’ 방식이 아닌, 약의 첫 적응증이 ‘코로나 19’라는 점에서 코로나 19 ‘신약’이라는 의의를 가진다.

[혈장분획치료제 제조공정 개요]
혈장분획치료제는, 코로나19 완치자의 혈장에 있는 코로나바이러스를 중화시킬 수 있는 항체를 농축시켜 만든다.
즉, 완치자를 채혈 후 혈장을 대량으로 모아 혈장 내 다른 성분과 중화항체가 포함된 면역글로불린을 분리, 정제 및 농축하여 불순물을 제거 후 제제화하여 ‘혈장분획치료제’를 생산한다. 채혈, 분리 등의 과정이 있기 때문에, 대량생산은 힘들다는 단점이 있다.
[녹십자의 GC5131 혈장분획치료제]
‘GC5131’은 코로나19 완치자의 혈장을 이용해 개발 중인 ‘고면역글로불린(Hyper-immune Globulin)’ 성분 의약품이다.
혈장이 인체에서 유래했다는 점과 중화항체를 이용해 치료하는 약들은 예전부터 사용됐다는 점을 고려해 식약처는 안전성을 평가하는 임상 1상 시험을 면제했다. GC5131는 바로 임상 2상 시험으로 들어가 치료목적승인을 받고, 국내 첫 코로나 19 치료제라는 별칭을 가지게 되었다.
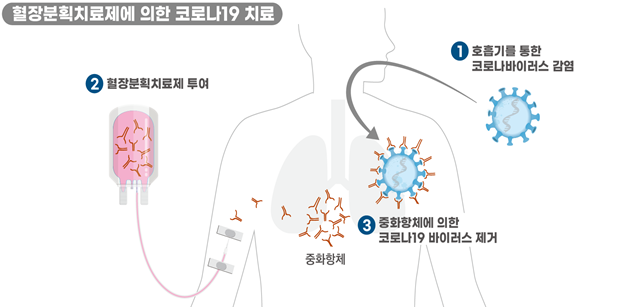
[혈장분획치료제 작용 원리]
투여된 중화항체가 몸에 침입한 ‘코로나19 바이러스’를 중화하여(바이러스를 둘러싸) 바이러스가 몸의 다른 부분과 작용하지 못하도록 한다. 일차적으로는 바이러스가 몸에 직접적으로 붙지 못하게 하기 때문에, 감염에 저항력을 줄 수 있다.
또한, 항체로 중화된 바이러스는 다른 면역세포에 의해 중화되지 않은 바이러스보다 더 빨리 제거될 수 있기 때문에 치료의 효과를 볼 수 있다.
[셀트리온의 유전자재조합 중화항체치료제 ‘CT-P59’]
지난 11일 ‘치료 목적 사용승인’을 받은 셀트리온의 ‘CT-P59’는 ‘유전자 재조합 중화항체치료제’다. ‘중화항체치료제’의 원리는 ‘혈장분획치료제’와 같다. ‘혈장분획치료제’와는 만드는 방식에서 차이점이 있는데, ‘CT-P59’는 바이러스 중화 능력이 강한 항체의 유전자를 세포에 삽입한 후, 세포를 배양해 생산한다. 따라서, 혈장분획치료제와는 달리 채혈하여 농축하는 방식이 아니기 때문에, 대량생산이 가능하다. 유전자를 삽입한 세포를 마치 공장처럼 이용하여 실험실에서 배양 및 생산하는 방식이기 때문에 대량생산이 가능하다.
또한, CT-P59는 경증 및 중등증 코로나-19 감염 환자의 치료목적으로 임상시험 승인을 받았다는 것과 코로나-19 감염 환자와 접촉한 사람에게 있어 예방적 유효성에 대해 임상시험 승인을 받은 것이 주목할 만하다.
<기사관련 문의사항: 필스앤필스약국(https://blog.naver.com/byw401401)>






